學員們瘋狂敲碗的課程將於4/15~4/16兩天將於嘉義市開班啦! 因已有數組團體報名,名額非常有限如有意願還請盡速報名 報名表請點我
詳細內容

CM CONSULTING
ISO顧問公司|成銘管理顧問協助您的企業獲取國際認證
訓練很昂貴,但若不訓練的代價更高。
成銘的團隊於管理顧問業界、工廠實務界皆有相當豐富經驗,善於處理客戶需求及實際執行上的困難點,看著公司藉由導入ISO國際管理系統或者教育訓練獲得提升,並能於產業界裡發光發熱是我們繼續向前走的動力。
感謝各大企業選擇成銘顧問,並給予正面、認同的評價。我們的服務不僅可符合第三方驗證單位的標準,更可為客戶達到品牌供應商的要求,這是一般同業難以承諾的,也是我們在顧問業屹立不搖的最大主因,因為我們相信,成功不二唯其銘。
ENTERPRISE SOLUTION
ISO顧問公司|成銘管理顧問協助您的企業獲取國際認證
國際標準更新脈動
因應國際趨勢及世界潮流的議題,所有的國際標準都會隨著時間作版本更新,成銘協助您在最快速的時間內掌握更新資訊。
成銘的專業團隊在各領域的系統標準發佈後,在最快的時間內透過翻譯團隊來得知未來版本的訴求重點,協助客戶在新舊版本更替時盡可能減少差異違和感及不便。
![]()
系統輔導ISO 9001、ISO 14001、ISO 22000、ISO 17025等其他顧問輔導
![]()
客戶稽核Costco 好市多、Walmart 沃爾瑪 、Nike 耐吉、社會責任驗廠
![]()
內訓課程能力培訓、內部稽核員、五大核心工具訓練、客製化課程
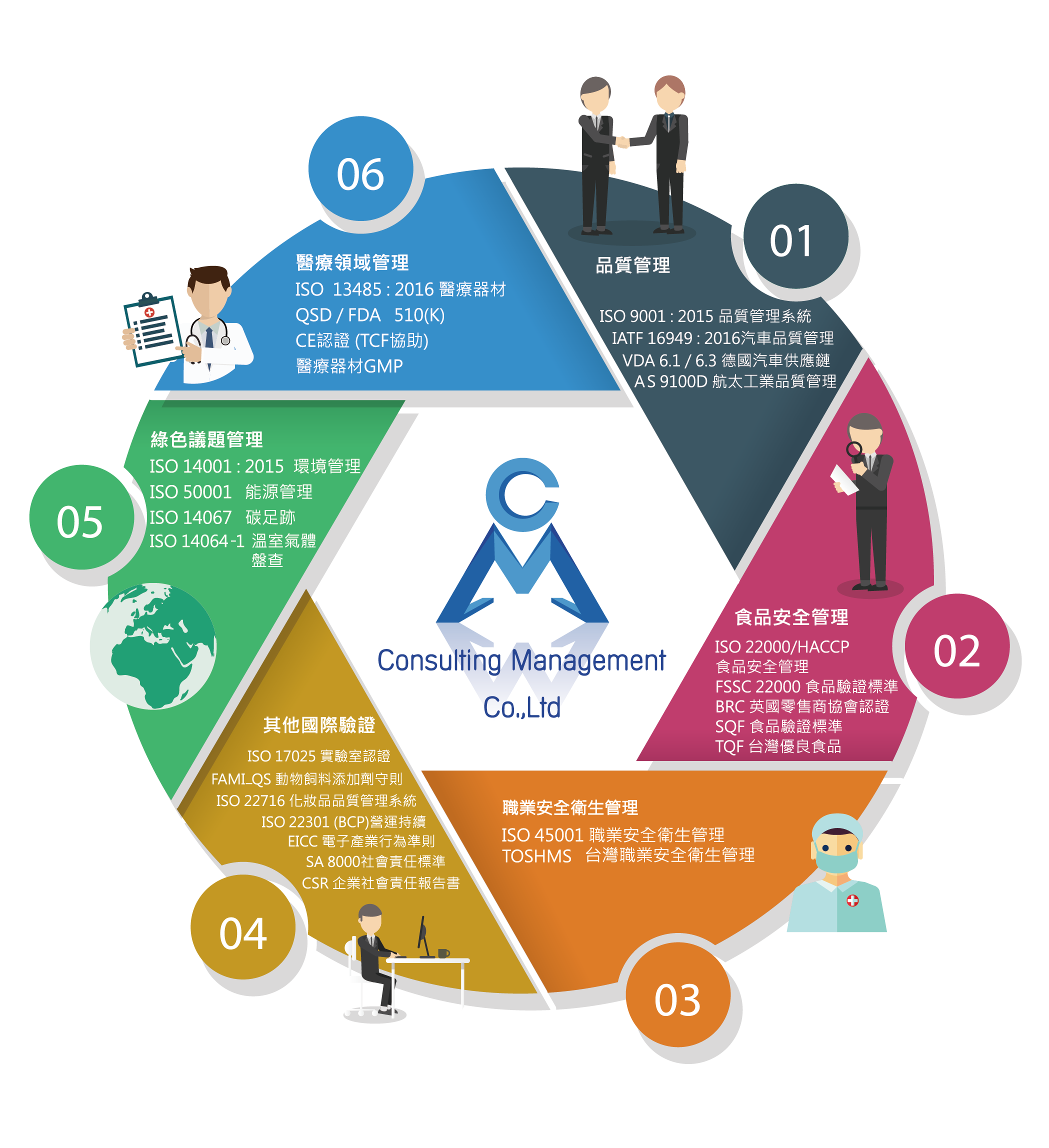
國際認證輔導服務項目
成銘專精各領域範圍![]()
品質保證
![]()
食品安全
![]()
實驗室
![]()
汽車領域
![]()
航太領域
![]()
醫療器材
![]()
環保議題
![]()
工作安全
![]()
資訊安全
![]()
企業營運
我們的認證輔導項目
解決方案服務流程
流程一. 需求、議題產生
可直接來信或致電成銘,將由專責人員接洽
流程二. 安排初訪
業務外勤人員拜訪、簡報
流程三. 專案討論
將所獲得之意見及方向帶回,與專屬領域顧問師討論並擬定計畫規格
流程四. 計畫定案
提供解決方案及報價規格書
流程五. 作業展開
進行輔導及訓練,完成最終專案目標
流程六. 售後服務
提供永久系統及國際標準諮詢,陪伴企業持續成長
產業文章及新訊
客戶見證實績
ISO顧問服務諮詢時間
感謝各大企業選擇成銘顧問,並給予正面、認同的評價。我們的服務不僅可符合第三方驗證單位的標準,更可為客戶達到品牌供應商的要求,這是一般同業難以承諾的,也是我們在顧問業屹立不搖的最大主因,因為我們相信,成功不二唯其銘。
- 周一-周五: 10AM to 7PM
- 周六: 11AM to 3PM
- 周日: Closed

